Das Märchen vom entfärbten Glas
Das in den deutschen Glashütten im Mittelalter und in der frühen Neuzeit erzeugte Gebrauchsglas war in der Regel mehr oder minder stark grün gefärbt. Die Bezeichnung »Waldglas« hierfür geht jedoch nicht auf die »waldgrüne« Färbung, sondern auf den Standort der Hütten im Walde zurück. Abbildung 1 zeigt einen Nuppenbecher aus leicht grünem Glas; es handelt sich um eine Replik aus Böhmen. Mehr oder minder farblose Nuppenbecher waren im 13./14. Jahrhundert weit verbreitet.
Die Färbung wird von Eisen verursacht, das in den verwendeten Rohstoffen (Holzasche, Sand oder Kiesel, ggf. Kalkstein) als Verunreinigung praktisch immer vorhandenen ist. Je nach der Eisenkonzentration und den Schmelzbedingungen werden blau- oder gelbstichige, starke oder schwache Grünfärbungen erhalten. In Abbildung 2 sind einige stärker grün gefärbte Glasfragmente gezeigt.
In der Regel war diese Färbung unerwünscht, und die Suche nach Methoden zur Herstellung farblosen Glases ist uralt, da auch schon antike römische Glashütten vor dem Problem standen.
Ein Weg hierzu – und sicherlich der beste – ist die Verwendung von wirklich eisenfreien Rohstoffen. Die venezianischen Glashütten verfügten hierüber dank ihres weit gespannten Handelsnetzes: die aus dem Orient bezogene Seepflanzenasche ist praktisch eisenfrei, auch die als Siliziumquelle dienenden schneeweißen Flusskiesel aus Norditalien weisen praktisch keine Eisenverunreinigung auf. Die Glashütten von Venedig konnten also ein farbloses Glas herstellen, das als »cristal de Venise« ab der frühen Neuzeit den Maßstab setzte. Die Herstellung von Glas dieser Spitzenqualität war ein Ziel der Glashütten. Da eisenfreie Rohstoffe jedoch selten verfügbar waren (die verwendete Holzasche war immer eisenhaltig, wie auch meistens der Sand), suchte man Verfahren zur Entfärbung von Glas.
Der Wunsch zur Herstellung farblosen Glases besteht – wie schon erwähnt - nicht erst seit dem Mittelalter; bereits antike römische Glashütten suchten nach Möglichkeiten hierzu.
Ein Weg wird bereits von Plinius d. Ä.
Agricola
Als nächste Autorität ist Kunckel
Es ist interessant, wie sich bei den drei erwähnten Autoren die Beobachtungen zunehmend konkretisieren; eine richtige Erklärung der Erscheinungen war jedoch auch Kunckel noch nicht möglich.
Dies gelang erst im 20. Jahrhundert, und hier ist die Arbeit von Sellner, Oel und Camara
Zunächst ist festzuhalten, dass Eisen im Glas in den Oxidationsstufen +2 und +3 vorkommen kann (früher sagte man »Wertigkeiten« hierzu). Eisen in der Oxidationsstufe +2 (geschrieben Eisen(II) ) verursacht eine Blaufärbung, Eisen in der Oxidationsstufe +3 (geschrieben Eisen(III) ) verursacht eine Gelbfärbung des Glases. Die Grünfärbung des »Waldglases« entsteht wegen seiner Gehalte an Eisen(II) und Eisen(III) als Mischfärbung aus Blau und Gelb. Die an den grünen Gläsern beobachteten Blau- bzw. Gelbstiche entstehen durch unterschiedliche Konzentrationsverhältnisse an Eisen(II) und Eisen(III). Abbildung 3 zeigt einen Glasbrocken aus einer rezenten Fehlcharge, der von Eisen(II) blau und von einem Eisen(II)-/ Eisen(III)-Gemisch grün gefärbte Bereiche, an manchen Stellen auch mit einem deutlichen Stich ins Gelbe, aufweist, weiterhin auch noch unumgesetzten weiß erscheinenden Quarz. Die verschiedenen Färbungen entstehen beim Niederschmelzen des Gemenges durch unbeabsichtigte Schwankungen des Sauerstoffgehaltes in der Ofenatmosphäre. Bei Ausgrabungen findet man manchmal schön blau gefärbte Glasfragmente, die sogar an Kobaltglas erinnern können, manchmal auch gelbes Glas, meist jedoch das übliche grüne Glas.
Die »Glasmacherseife« Braunstein ist chemisch Mangan(IV)-oxid. Es ist in geschmolzenem Glas unlöslich. Wird dieses Oxid des Mangans (Oxidationsstufe +4) in der geschmolzenen Glasmasse erhitzt, zerfällt es in Mangan(III)-oxid (Oxidationsstufe +3) und Sauerstoff. Mangan(III) färbt Glas stark rotviolett, und der Sauerstoff oxidiert das im Glas vorhandene Eisen(II) zu Eisen(III). Agricolas Bemerkung, dass der Braunstein vom Eisen verzehrt wird, hat also tatsächlich einen wahren Kern. Die miteinander verbundenen Oxidations- und Reduktionsprozesse konnte er zu seiner Zeit natürlich noch nicht verstehen. Die beiden damit im Glas nebeneinander vorliegenden Farben Gelb und Rotviolett haben nun die bemerkenswerte und wichtige Eigenschaft, sich als Komplementärfarben spektral zu ergänzen. Abbildung 4 verdeutlicht die Zusammenhänge.
In der Abbildung 4 sind eine von Eisen(III) gelb gefärbte und eine von Mangan(III) rotviolett gefärbte Glasplatte in der Mitte teilweise übereinander gelegt. Hier resultiert als Mischfarbe ein leicht violettstichiges Grau. Es entsteht dadurch, dass die Komplementärfarben zusammen über den ganzen Spektralbereich verteilt Anteile aus dem durchfallenden Licht herausnehmen: aus »Weiß« wird »Grau«. Der Physiker nennt dies eine subtraktive Farbmischung, weil Lichtanteile aus dem einfallenden weißen Licht herausgenommen, von ihm »subtrahiert«, werden.
Kunckels Beobachtung, dass die Färbung ins Schwärzliche übergeht, ist also völlig richtig, und man kann tatsächlich an vielen alten Gläsern einen Grauton bemerken. Dies ist besonders dann der Fall, wenn das Glas stark eisenhaltig war und also auch viel Braunstein zugesetzt werden musste.
Der Farbstich des Grau hat seinen Grund darin, dass die Farbintensitäten der beiden zur Verfügung stehenden Glasplatten nicht genau aufeinander abgestimmt sind. Auch diese Beobachtung ist an vielen alten Gläsern zu machen: auch die alten Glaser hatten mit dem Problem der Farbstiche zu kämpfen; sie mussten die zuzusetzenden Braunsteinmengen durch Vorversuche ermitteln und waren auf ihre Erfahrung angewiesen. Dabei gelang es nicht immer, den Braunsteinzusatz genau auf den Eisengehalt abzustimmen.
Hier muss also festgehalten werden, dass das Glas nicht entfärbt, sondern die Grünfärbung nur durch Umwandlung in eine wenig auffallende Graufärbung maskiert wird. Es ist falsch, von einer Entfärbung des Glases zu sprechen.

Es gibt noch eine andere Möglichkeit, die Grünfärbung weniger deutlich erkennen zu lassen, die ebenfalls genutzt wurde. Sie beruht auf der für die verschiedenen Farben unterschiedlichen Empfindlichkeit des menschlichen Auges. Unser Auge ist am empfindlichsten für die Farbe »grün« (genau: die Lichtwellenlänge 555 nm); seine Empfindlichkeit ist an den Enden des sichtbaren Spektrums, also im Blauen und Violetten einerseits und im Gelben und Roten andererseits, deutlich niedriger. Wenn es gelingt, das deutlich erkennbare Grün des Glases in eine weniger deutlich erkennbare Farbe, z. B. in ein stark verweißlichtes Gelb, umzuwandeln, erzielt man den scheinbaren Effekt einer »Entfärbung«, die in der Realität natürlich keine ist.
Tabelle 1 soll diesen Effekt verdeutlichen. Der gleiche Text wurde in zwei Farben geschrieben, die so ausgewählt wurden, dass sie die gleiche Intensität und die gleiche Sättigung aufweisen. Es zeigt sich, dass der grüne Text leichter zu lesen ist als der gelbe. Die alten Glaser fanden nun tatsächlich eine Möglichkeit, diesen Effekt auszunutzen. Sie setzten der Glasschmelze Arsen(III)-oxid zu, das in der Schmelze durch den Luftsauerstoff zu Arsen(V)-oxid oxidiert wird. Dieses ist nun seinerseits in der Lage, das vorhandene Eisen(II) zu Eisen(III) zu oxidieren ohne selbst eine Färbung zu verursachen. Hierdurch wandelt sich die grüne Färbung des Glases in eine gelbe um: das Glas wurde zwar nicht entfärbt, aber seine Färbung ist weniger deutlich zu erkennen.
Auch bei dieser Vorgehensweise wird das Glas also nicht entfärbt, sondern lediglich umgefärbt. Auch hier ist es falsch, von einer Entfärbung des Glases zu sprechen.
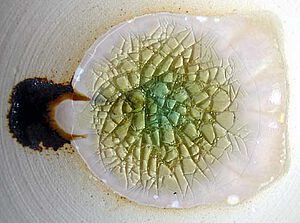
Um die Beweiskette vollends zu schließen, wurde nun noch der Versuch unternommen, grünes Glas in gelbes umzuwandeln – nur durch Erhitzen an der Luft. Dieser Versuch soll also demonstrieren, dass der Luftsauerstoff in der Lage ist, Eisen(II) in der Glasschmelze zu Eisen(III) zu oxidieren. Hierzu wurde eine Scherbe eines grünen Waldglases auf einem weißen Keramikteller in einem Elektroofen bei freiem Luftzutritt auf 1300 °C erhitzt. Die Aufheizzeit betrug 5 Stunden, die Haltezeit dieser Temperatur 7 Stunden. Abbildung 5 zeigt das Ergebnis.
Nach diesem Prozess war die erstarrte Schmelze also tatsächlich gelb geworden, lediglich in der Mitte war noch etwas vom ursprünglichen Grün zu sehen. Die milchigweißen Zonen sind Bereiche, in denen Kristallisation erfolgte – eine in diesem Zusammenhang bedeutungslose Begleiterscheinung.
Wichtig ist, dass Luftsauerstoff in der Lage ist, das Eisen(II) im grünen Glas zu Eisen(III) zu oxidieren. Dieser Prozess dauert relativ lange, weil der Sauerstoff in die recht zähe Glasschmelze eindiffundieren muss, was einige Zeit beansprucht
Zusammenfassend ist also zu sagen:
Das grüne Waldglas ist nicht zu entfärben. Die Grünfärbung kann lediglich maskiert werden, was zu einer wenig auffälligen Graufärbung führt, oder sie kann durch Umwandlung in eine weniger gut erkennbare Gelbfärbung getarnt werden.
Wirklich farbloses Glas lässt sich nur durch Verwendung praktisch eisenfreier Rohstoffe erzeugen.
Wenn in der Literatur von „entfärbtem“ Glas die Rede ist, verbreitet der betreffende Autor ein Märchen, das keinen naturwissenschaftlichen Hintergrund besitzt.
Literatur
Agricola 1557
Georgius Agricola, De re metallica, Basel 1557.
Kunckel 1679
Johann Kunckel, Ars vitraria experimentalis. J. Kunckels Anmerckungen über das 1. Buch Anthonii Neri von der Glaskunst, 1679.
Kurzmann 2004
Peter Kurzmann, Mittelalterliche Glastechnologie, Frankfurt am Main 2004.
Plinius d. Ä. 2. Hälfte 1. Jh. n. Chr.
Plinius Secundus d. Ä., Naturalis Historia 36, 192. Übersetzt und kommentiert von der Projektgruppe Plinius. Rolf C. A. Rottländer (Hrsg.), Über Glas und Metalle, St. Katharinen 2000.
Sellner, Oel, Camara 1979
Christiane Sellner, Heribert J. Oel, Boubacar Camara, Untersuchung alter Gläser (Waldglas) auf Zusammenhang von Zusammensetzung, Farbe und Schmelzatmosphäre mit der Elektronenspektroskopie und der Elektronenspinresonanz (ESR), Glastechnische Berichte 52, 1979.
Fußnoten
An dieser Stelle sei erwähnt, dass die starke Grünfärbung rezenter Weinflaschen nicht durch Eisen verursacht wird, sondern durch Chrom. ↩
Plinius d. Ä., 2. Hälfte 1. Jh. n. Chr., 36, 192. ↩
Agricola, 1557, 12. Buch, 484. ↩
Kunckel, 1679, Anmerkungen über das 1. Buch Neri, 55-56. ↩
Sellner, Oel, Camara 1979, 255-64. ↩
Kurzmann 2004, 205-217. ↩




